Для работы любой тепловой машины по замкнутому циклу необходима внешняя среда, которую условно можно представить себе как два тела - нагреватель Т mах, и холодильник , находящийся при температуре T min (T min < Т mах ). Предполагается, что при контакте с нашей системой температуры нагревателя и холодильника не меняются. При контакте с нагревателем система получает тепло, при контакте с холодильником - отдает его.
В термодинамике существует теорема Карно (рис. 5.2):
Рис. 5.2. Леонар Сади Карно (французский физик и военный инженер)
|
При заданных температурах нагревателя и холодильника максимально возможный КПД тепловой машины не зависит от природы рабочего тела машины и определяется формулой
|
Реализация максимально возможного КПД достигается в так называемом цикле Карно , когда идеальный газ проходит замкнутый цикл, составленный из двух адиабат и двух изотерм (рис. 5.3).

Рис. 5.3. Цикл Карно (обходится по часовой стрелке) - комбинация двух изотерм 1 - 2, 3 - 4 и двух адиабат 2 - 3 и 4 - 1 ; теплообмен со средой осуществляется на изотермических участках цикла: на участке 1 - 2 газ получает теплоту Q 1 , а на участке 3 - 4 отдает теплоту Q 2
Убедимся, что показанный замкнутый процесс действительно имеет КПД, соответствующий формуле (5.5). Температура системы равна T 1 в точках 1, 2 и T 2 в точках 3, 4 . Значения остальных термодинамических параметров (р, V) будут иметь в качестве индекса номер соответствующей точки на диаграмме. Нам надо вычислить количества полученной Q 1 , и отданной Q 2 теплоты, найти совершенную газом работу А Ц = Q 1 – Q 2 и определить КПД цикла. Сразу заметим, что на участках 2-3 и 4-1 система не обменивается теплом с внешней средой. Следовательно, теплоту Q 1 газ получает на участке 1-2, а теплоту Q 2 отдает на участке 3-4. Рассмотрим подробнее различные участки цикла.
Изотерма 1 -2. На этом участке газ находится в контакте с нагревателем и происходит изотермическое расширение от объема V 1 до объема V 2 . Температура Т 1 не меняется, следовательно, не изменяется внутренняя энергия, а вся полученная теплота расходуется на совершение газом работы:
![]()
Величину работы газа при изотермическом процессе мы уже вычисляли ранее, так что с учетом формулы (2.13) находим
находим
|
|
Адиабата 2 -3. Здесь система отсоединяется от нагревателя и не обменивается теплом с внешней средой: Q 23 = 0 . Газ продолжает расширяться, но уже адиабатно. Работа совершается за счет внутренней энергии газа, и его температура падает до значения Т 2 . На этом участке цикла нам нужна информация, доставляемая уравнением адиабаты :
|
|
Изотерма 3 -4. Система подключается к холодильнику, и газ начинает сжиматься. Внутренняя энергия остается неизменной, над газом совершается работа (А 34 < 0 ), а выделяющееся
![]()
передается холодильнику. Имеем аналогично (5.6)
|
|
Адиабата 4 -1. Система отключена от внешней среды и продолжает сжиматься изотермически, что приводит к повышению ее температуры до Т 1 . В конечном итоге система возвращается в первоначальное состояние. Поскольку точки 4 и 1 лежат на адиабате, получаем связь объемов и температур, аналогичную (5.7):
|
|
Из уравнений (5.7) и (5.9) находим отношения объемов

откуда следует, что
Поэтому отдаваемую холодильнику теплоту Q 2 (см. уравнение (5.8)) можно записать как
|
|
Используя выражение (5.6) для теплоты, полученной системой, находим совершенную в ходе цикла работу
|
|
Из проведенного анализа следует также, что максимальная температура в цикле равна Т mах = Т 1 , а минимальная - Т min = Т 2 . Если разделить (5.12) на (5.6), то немедленно получим выражение (5.5) для КПД цикла Карно, из которого выпадают все параметры, кроме температур холодильника и нагревателя.
Пример 1. Котел тепловой станции работает при температуре около t 1 = 550 °С . Отработанное тепло отводится к реке при температуре около t 2 = 20 °С . Найдем максимально возможный КПД этой станции (рис. 5.4).

Рис. 5.4. Схема работы тепловой машины Карно
Поскольку в формуле для КПД цикла Карно используются абсолютные температуры, надо перейти от шкалы Цельсия к шкале Кельвина: Т 1 = 550 + 273 = 823 К , Т 2 = 20 + 273 = 293 К . Теперь находим КПД тепловой станции:
![]()
Конечно, реальный КПД станции заметно ниже.
Если цикл Карно осуществить в обратном направлении, то есть против часовой стрелки на рис. 5.2, то для определения эффективности холодильной установки надо использовать формулы (5.3), (5.4) и выражения (5.6), (5.11). Получаем тогда
|
|
Печально, но чем ниже температура внешней среды Т 1 , тем меньше мы нуждаемся в холодильнике, и тем эффективнее он работает.

Рис. 5.5. Схема работы холодильной установки
Приведем численный пример. Если кондиционер поддерживает в комнате температуру t 2 = 20 °С , а температура наружного воздуха равна t 1 = 30 °С , то для холодильного коэффициента имеем

а для КПД холодильника

Конечно, на самом деле температура тепловыделяющего элемента больше наружной температуры на 20–30 градусов, так что разность температур может достигать 30–40 градусов, что приводит к значениям

Напомним, что речь идет об идеальных установках, работающих по циклу Карно. Реальный типичный кондиционер потребляет мощность 750 Вт , перекачивая за час около 5 МДж тепловой энергии. Это значит, что за секунду кондиционер совершает работу А = 750 Дж и отнимает у воздуха в комнате теплоту

Отсюда находим
Мы видим, что реальный кондиционер гораздо менее эффективен, нежели идеальный холодильник Карно.
Пример 2. Пусть в домашнем холодильнике поддерживается температура t 2 = –3 °С (Т 2 = 270 К ), а температура в кухне равна t 1 = 27 °С (T 1 = 300 К ). Пусть далее мотор холодильника потребляет мощность N = 200 Вт . Предполагая, что холодильник работает по циклу Карно и что тепловыделяющий элемент имеет температуру окружающего воздуха, определим мощность потока тепловой энергии, перекачиваемой из камеры холодильника в кухню.
За время t мотор совершит работу
КПД холодильника равен

откуда находим количество теплоты, поступающее в кухню в единицу времени:
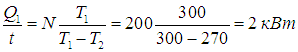
Обратите внимание, что холодильник работает как весьма эффективный обогреватель помещения. Надо только оплачивать потребляемую мотором мощность 200 Вт , а в кухню поступит в 10 раз большая энергия, 90 % которой перекачивается из камеры холодильника (90 % - КПД холодильника в этом примере). Любопытно, что если бы вместо холодильника был включен обогреватель той же мощности, то он нагревал бы помещение в 10 раз слабее.
Наши численные оценки можно рассматривать как пример теплового загрязнения окружающей среды, свойственного технической цивилизации.
Дополнительная информация
http://eqworld.ipmnet.ru/ru/library/physics/thermodynamics.htm - Я. де Бур Введение в молекулярную физику и термодинамику, Изд. ИЛ, 1962 г. - стр. 202–205, ч. 2, гл. 2, § 10: описан процесс ожижения газа Клода - Гейландта.§6 Энтропия
Обычно всякий процесс, при котором система переходит из одного состояния в другое, протекает таким образом, что нельзя провести этот процесс в обратном направлении так, чтобы система проходила через те же промежуточные состояния, и при этом в окружающих телах не произошли какие-либо изменения. Это связано с тем, что в процессе часть энергии рассеивается, например, за счет трения, излучения и т. п. Т. о. практически все процессы в природе необратимы. В любом процессе часть энергии теряется. Для характеристики рассеяния энергии вводится понятие энтропии. (Величина энтропии характеризует тепловое состояние системы и определяет вероятность осуществления данного состояния тела. Чем более вероятно данное состояния, тем больше энтропия.) Все естественные процессы сопровождаются ростом энтропии. Энтропия остается постоянной только в случае идеализированного обратимого процесса, происходящего в замкнутой системе, то есть в системе, в которой не происходит обмен энергией с внешними по отношению к этой системе телами.
Энтропия и ее термодинамический смысл:
Энтропия - это такая функция состояния системы, бесконечно малое изменение которой в обратимом процессе равно отношению бесконечно малого количества теплоты, введенного в этом процессе, к температуре, при которой оно вводилось.
В конечном обратимом процессе изменения энтропии может быть подсчитано по формуле:
![]()
где интеграл берется от начального состояния 1 системы до конечного состояния 2.
Поскольку энтропия есть функция состояния, то свойством интеграла является его независимость от формы контура (пути), по которому он вычисляется, следовательно, интеграл определяется только начальным и конечным состояниям системы.
- В любом обратимом процессе изменения энтропии равно 0
(1)
- В термодинамике доказывается, что S системы совершающей необратимой цикл возрастает
Δ S > 0 (2)
Выражения (1) и (2) относятся только к замкнутым системам, если же система обменивается теплотой с внешней средой, то её S может вести себя любым образом.
Соотношения (1) и(2) можно представить в виде неравенства Клаузиуса
Δ S ≥ 0
т.е. энтропия замкнутой системы может либо возрастать (в случае необратимых процессов) либо оставаться постоянной (в случае обратимых процессов).
Если система совершает равновесный переход из состояния 1 в состояния 2, то изменения энтропии
![]()
где dU и δA записывается для конкретного процесса. По этой формуле Δ S определяется с точностью до аддитивной постоянной. Физический смысл имеет не сама энтропия, а разность энтропий. Найдем изменение энтропии в процессах идеального газа.
![]()
т.е. изменения энтропии S Δ S 1→2 идеального газа при переходе его из состояния 1 в состояния 2 не зависит от вида процесса.
Т.к. для адиабатического процесса δ Q = 0, то Δ S = 0 => S = const , то есть адиабатический обратимый процесс протекает при постоянной энтропии. Поэтому его называют изоэнтропийным.
При изотермическом процессе (T = const ; T 1 = T 2 : )
![]()
При изохорном процессе (V = const ; V 1 = V 2 ; )
![]()
Энтропия обладает свойством аддитивности: энтропия системы равна сумме энтропий тел входящих в систему. S = S 1 + S 2 + S 3 + ... Качественным отличием теплового движения молекул от других форм движения является его хаотичность, беспорядочность. Поэтому для характеристики теплового движения необходимо ввести количественную меру степени молекулярного беспорядка. Если рассмотреть какое-либо данное макроскопическое состояния тела с определенными средними значениями параметров, то оно есть нечто иное, как непрерывная смена близких микросостояний, отличающихся друг от друга распределением молекул в разных частях объема и распределяемой энергией между молекулами. Число этих непрерывно сменяющих друг друга микросостояний характеризует степень беспорядочности макроскопического состояния всей системы, w называется термодинамической вероятностью данного микросостояния. Термодинамическая вероятность w состояния системы — это число способов, которыми может быть реализовано данное состояния макроскопической системы, или число микросостояний, осуществляющих данное микросостояния (w ≥ 1, а математическая вероятность ≤ 1 ).
За меру неожиданности события условились принимать логарифм его вероятности, взятый со знаком минус: неожиданность состояния равна = -
Согласно Больцману, энтропия S системы и термодинамическая вероятность связаны между собой следующим образом:
где
- постоянная Больцмана (![]() ). Таким образом, энтропия определяется логарифмом числа состояния, с помощью которых может быть реализовано данное микросостояние. Энтропия может рассматриваться как мера вероятности состояния т/д системы. Формула Больцмана позволяет дать энтропии следующее статистическое толкования. Энтропия является мерой неупорядоченности системы. В самом деле, чем больше число микросостояний реализующих данное микросостояние, тем больше энтропия. В состоянии равновесия системы - наиболее вероятного состояния системы - число микросостояний максимально, при этом максимальна и энтропия.
). Таким образом, энтропия определяется логарифмом числа состояния, с помощью которых может быть реализовано данное микросостояние. Энтропия может рассматриваться как мера вероятности состояния т/д системы. Формула Больцмана позволяет дать энтропии следующее статистическое толкования. Энтропия является мерой неупорядоченности системы. В самом деле, чем больше число микросостояний реализующих данное микросостояние, тем больше энтропия. В состоянии равновесия системы - наиболее вероятного состояния системы - число микросостояний максимально, при этом максимальна и энтропия.
Т.к. реальные процессы необратимы, то можно утверждать, что все процессы в замкнутой системе ведут к увеличению ее энтропии - принцип возрастания энтропии. При статистическом толковании энтропии это означает, что процессы в замкнутой системе идут в направлении увеличения числа микросостояний, иными словами, от менее вероятных состояний к более вероятным, до тех пор, пока вероятность состояния не станет максимальной.
§7 Второе начало термодинамики
Первое начало термодинамики, выражая закон сохранения энергии и превращения энергии, не позволяет установить направление протекания т/д процессов. Кроме того, можно представить множество процессов, не противоречащих I началу т/д, в которых энергия сохраняется, а в природе они не осуществляются. Возможные формулировки второго начало т/д:
1) закон возрастания энтропии замкнутой системы при необратимых процессах: любой необратимой процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает Δ S ≥ 0 (необратимый процесс) 2) Δ S ≥ 0 (S = 0 при обратимом и Δ S ≥ 0 при необратимом процессе)
В процессах, происходящих в замкнутой системе, энтропия не убывает.
2) Из формулы Больцмана S = , следовательно, возрастание энтропии означает переход системы из менее вероятного состояния в более вероятное.
3) По Кельвину: не возможен круговой процесс, единственным результатом которого является превращения теплоты, полученной от нагревателя в эквивалентную ей работу.
4) По Клаузиусу: не возможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому.
Для описания т/д систем при 0 К используют теорему Нернста-Планка (третье начало т/д): энтропия всех тел в состоянии равновесия стремится к нулю по мере приближения температуры к 0 К
Из теоремы Нернста-Планка следует, что C p = C v = 0 при 0 К
§8 Тепловые и холодильные машины.
Цикл Карно и его к.п.д.
Из формулировки второго начала т/д по Кельвину следует, что вечный двигатель второго рода невозможен. (Вечный двигатель - это периодически действующий двигатель, совершающий работу за счет охлаждения одного источника теплоты.)
 Термостат
- это т/д система, которая может обмениваться теплотой с телами без изменения температуры.
Термостат
- это т/д система, которая может обмениваться теплотой с телами без изменения температуры.
Принцип действия теплового двигателя: от термостата с температурой Т 1 - нагревателя, за цикл отнимается количество теплоты Q 1 , а термостату с температурой Т 2 (Т 2 < Т 1) -холодильнику, за цикл передается количество теплоты Q 2 , при этом совершается работа А = Q 1 - Q 2
 Круговым процессом или циклом
называется процесс, при котором система, пройдя через ряд состояний, возвращается в исходное. На диаграмме состояний цикл изображается замкнутой кривой. Цикл, совершаемый идеальным газом, можно разбить на процессы расширения (1-2) и сжатия (2-1), работа расширения положительна А
1-2 > 0, т.к.
V
2
>
V
1
, работа сжатия отрицательна А
1-2 < 0, т.к.
V
2
<
V
1
. Следовательно, работа совершаемая газом за цикл, определяется площадью, охватываемой замкнутой кривой 1-2-1. Если за цикл совершается положительная работа (цикл по часовой стрелке), то цикл называется прямым, если - обратный цикл (цикл происходит в направлении против часовой стрелки).
Круговым процессом или циклом
называется процесс, при котором система, пройдя через ряд состояний, возвращается в исходное. На диаграмме состояний цикл изображается замкнутой кривой. Цикл, совершаемый идеальным газом, можно разбить на процессы расширения (1-2) и сжатия (2-1), работа расширения положительна А
1-2 > 0, т.к.
V
2
>
V
1
, работа сжатия отрицательна А
1-2 < 0, т.к.
V
2
<
V
1
. Следовательно, работа совершаемая газом за цикл, определяется площадью, охватываемой замкнутой кривой 1-2-1. Если за цикл совершается положительная работа (цикл по часовой стрелке), то цикл называется прямым, если - обратный цикл (цикл происходит в направлении против часовой стрелки).
Прямой цикл используется в тепловых двигателях - периодически действующих двигателях, совершающих работу за счет полученной извне теплоты. Обратный цикл используется в холодильных машинах - периодически действующих установках, в которых за счет работы внешних сил теплота переносится к телу с более высокой температурой.
В результате кругового процесса система возвращается в исходное состояние и, следовательно, полное изменение внутренней энергии равно нулю. Тогда І начало т/д для кругового процесса
Q = Δ U + A = A ,
Т. е. работа, совершаемая за цикл равна количеству полученной извне теплоты, но
Q = Q 1 - Q 2
Q 1 - количество теплоты, полученное системой,
Q 2 - количество теплоты, отданное системой.
Термический к.п.д. для кругового процесса равен отношению работы, совершенной системой, к количеству теплоты, подведенному к системе:
![]()
Чтобы η = 1, должно выполняться условие Q 2 = 0, т.е. тепловой двигатель должен иметь один источник теплоты Q 1 , но это противоречит второму началу т/д.
Процесс обратный происходящему в тепловом двигателе, используется в холодильной машине.
 От термостата с температурой Т
2 отнимается количество теплоты
Q
2
и передается термостату с температурой
T
1
, количество теплоты
Q
1
.
От термостата с температурой Т
2 отнимается количество теплоты
Q
2
и передается термостату с температурой
T
1
, количество теплоты
Q
1
.
Q = Q 2 - Q 1 < 0, следовательно A < 0.
Без совершения работы нельзя отбирать теплоту от менее нагретого тела и отдавать ее более нагретому.
Основываясь на втором начале т/д, Карно вывел теорему.
Теорема Карно: из всех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей (Т 1) и холодильников (Т 2), наибольшим к.п.д. обладают обратимые машины. К.П.Д. обратимых машин при равных Т 1 и Т 2 равны и не зависят от природы рабочего тела.
Рабочее тело - тело, совершающее круговой процесс и обменивающиеся энергией с другими телами.
Цикл Карно - обратимый наиболее экономичный цикл, состоящий из 2-х изотерм и 2-х адиабат.
 1-2-изотермическое расширения при Т
1 нагревателя; к газу подводится теплота
Q
1
и совершается работа
1-2-изотермическое расширения при Т
1 нагревателя; к газу подводится теплота
Q
1
и совершается работа
![]()
2-3 - адиабат. расширение, газ совершает работу A 2-3 >0 над внешними телами.
3-4-изотермическое сжатие при Т
2 холодильника; отбирается теплота
Q
2
и совершается работа
![]() ;
;
4-1-адиабатическое сжатие, над газом совершается работа A 4-1 <0 внешними телами.
При изотермическом процессе U = const , поэтому Q 1 = A 12
![]() 1
1
При адиабатическом расширении Q 2-3 = 0, и работа газа A 23 совершается за счет внутренней энергии A 23 = - U
![]()
Количество теплоты Q 2 , отданное газом холодильнику при изотермическом сжатии равно работе сжатия А 3-4
![]() 2
2
Работа адиабатического сжатия
![]()
Работа, совершаемая в результате кругового процесса
A = A 12 + A 23 + A 34 + A 41 = Q 1 + A 23 - Q 2 - A 23 = Q 1 - Q 2
и равна площади кривой 1-2-3-4-1.
Термический к.п.д. цикла Карно
![]()
Из уравнения адиабаты для процессов 2-3 и 3-4 получим
Тогда
![]()
![]()
т.е. к.п.д. цикла Карно определяется только температурами нагревателя и холодильника. Для увеличения к.п.д. нужно увеличивать разность Т 1 - Т 2 .
******************************************************* ******************************************************
Пусть в результате некоторого процесса система (ТДС) переходит из состояния 1 в состояние 2. Все процессы перехода системы можно разделить на два вида: 1) обратимые 2) и необратимые процессы.
Процесс 1→2 называется обратимым, если можно осуществить обратный переход 2→1 через те же промежуточные состояния в исходное состояние таким образом, чтобы состояние системы и тел вне системы осталось неизменным.
Процесс 1→2 называется необратимым, если после обратного процесса 2→1 в окружающих систему телах, либо в самой системе произошли какие-то изменения.
Отсутствие изменений в окружающей систему среде, является важной особенностью обратимого процесса. Если в ходе обратимого процесса система выполнила работу A за счет количества теплоты Q , полученного от окружающих ее тел, то при возвращении в первоначальное состояние, она должна отдать окружающим телам такое же количество теплоты Q и над ней должна быть выполнена такая же работа A .
Любой процесс, сопровождающийся трением, является необратимым, потому что в результате трения часть механической энергии переходит в теплоту, которая идет на нагревание трущихся тел. Это тепло рассеивается в окружающей среде и трущиеся, тела не могут сами по себе отдать это тепло в обратном процессе перехода.
Если силы трения очень малы, то процессы могут быть весьма близкими к обратимым. Например, колебания тяжелого маятника, удар стального шарика о массивную стальную плиту.
Необратимыми являются процессы, сопровождающиеся явлением теплопередачи, потому что переход теплоты от холодного тела к горячему не может происходить самопроизвольно. Для осуществления таких процессов требуется работа со стороны внешних тел, что приводит к изменениям в их состоянии, при этом утрачивается условие обратимости.
Необратимым является также процесс расширения газа в пустоту. При этом газ не испытывает сопротивления и не выполняет работу. Однако собрать газ обратно в сосуд без выполнения работы внешними телами невозможно.
Очевидно, что обратимыми могут быть только равновесные (квазистатические) процессы. При протекании равновесных процессов каждое промежуточное состояние является равновесным (состояние термодинамического равновесия) и, поэтому процесс может протекать в обратном направлении так, что в окружающих систему телах не останется никаких изменений. Обратимыми можно считать все изопроцессы.
I начало термодинамики устанавливает количественные соотношения между теплотой, работой и изменением внутренней энергии. Однако оно не указывает направление протекания процессов и не отвечает на вопрос о возможности протекания того либо иного процесса.
Согласно первому началу термодинамики в изолированной системе возможен процесс самопроизвольного перехода теплоты от холодного тела к горячему, главное чтобы при этом выполнялось равенство:
где Q 1 – количество теплоты, отданное первым телом, Q 2 – количество теплоты, полученное вторым телом.
Однако многочисленные опыты показывают, что теплота самопроизвольно переходит от горячего тела к холодному и никогда самопроизвольно наоборот.
Существует множество процессов в природе, которые самопроизвольно протекают только в строго определенном направлении: диффузия, расширение газа в пустоту, остывание нагретого тела и т.д.
I начало термодинамики не запрещает протекание этих процессов в обратном направлении, главное, чтобы при этом, не нарушался закон сохранения энергии .
Ответ на вопрос о возможности протекания того или иного процесса, о направлении протекания процессов дает второе начало термодинамики. II начало термодинамики, как и I начало, является обобщением многочисленных опытов.
II начало термодинамики – фундаментальный закон природы. Он охватывает все явления, которые связаны с обменом энергией и имеет глубокие практические и философские следствия.
Клаузиус: 1) Теплота не может сама собой перейти от менее нагретого тела к более нагретому . 2) Энтропия любой изолированной системы стремится к максимуму .
Кельвин (Томсон): Нельзя построить тепловую машину, которая превращала бы в работу теплоту наиболее холодного тела в системе .
Планк: Нельзя построить периодически действующую машину, единственным результатом работы которой было бы превращение теплоты в работу (важно периодически , т.к. при изотермическом процессе ΔU 12 = 0 и Q 12 = A 12 , но это будет однократный процесс).
Оствальд: Невозможно построить вечный двигатель второго рода .
Карно: Коэффициент полезного действия (КПД) идеальной тепловой машины не зависит от рода рабочего тела и определяется только температурами теплоотдатчика и теплоприемника .

Процессы, не противоречащие первому закону термодинамики, но запрещаемые вторым законом: 1 – «вечный двигатель второго рода»; 2 – самопроизвольный переход тепла от холодного тела к более теплому («идеальная холодильная машина»).
Практически все формулировки II начала термодинамики касаются тепловой машины. Рассмотрим принцип ее действия.
Процесс, при котором ТДС после ряда изменений состояния возвращается в первоначальное состояние, называется круговым процессом или циклом .
Тепловая машина это устройство , многократно выполняющее какой-либо круговой процесс и преобразующее теплоту в работу .
Работа, которая выполняется при круговом процессе, численно равна площади, охватываемой кривой, описывающей этот цикл (рис.1).

Рис.1. Термодинамический цикл тепловой машины
Эта работа положительная при прямом цикле 1a 2b 1 и отрицательная при обратном цикле 1b 2a 1. Любая тепловая машина независимо от ее конструкции состоит из трех основных частей: нагреватель, рабочее тело, холодильник.
Принцип действия тепловых машин заключается в следующем. Нагреватель передает рабочему телу теплоту, вызывая повышение его температуры. Рабочее тело совершает работу над каким-либо механическим устройством, например, приводит во вращение турбину или перемещает поршень в цилиндре и далее отдает холодильнику теплоту, возвращаясь в исходное состояние.
Машина, в которой рабочим телом служит идеальный газ, называется идеальной тепловой машиной. Тепловые машины могут работать по прямому или обратному циклу.
Рассмотрим схему машины, работающей по прямому циклу рис.2.

Рис.2. Энергетическая схема тепловой машины: 1 – нагреватель; 2 – холодильник; 3 – рабочее тело, совершающее круговой процесс.
Рабочее тело получает от нагревателя количество теплоты Q 1 . При этом оно расширяется по кривой 1a 2 (рис.1) и выполняет работу A . Чтобы цикл замкнулся рабочее тело необходимо перевести в первоначальное состояние 1. Для этого его надо сжать. Для сжатия необходимо совершить над рабочим телом работу. Для того чтобы работа, выполняемая при сжатии, была меньше, чем работа, выполненная при расширении, сжатие необходимо вести по кривой 2b 1. Следовательно, сжатие надо вести при более низкой температуре, чем температура нагревателя T 1 . Поэтому необходимо отнять у рабочего тела часть тепла Q 2 и передать ее холодильнику. В результате кругового процесса изменение внутренней энергии рабочего тела будет равно нулю:
![]()
Тогда согласно I началу термодинамики работа, совершенная рабочим телом за цикл равна разности подведенной и отведенной теплоты:
![]() (1)
(1)
Экономичность работы тепловых машин характеризуется коэффициентом полезного действия КПД , который показывает, какая часть полученной теплоты преобразовалась в работу. КПД равен отношению работы A , выполненной за цикл к количеству теплоты, полученной машиной за цикл:
 (2)
(2)
Рассмотрим работу тепловой машины по обратному циклу


Рис.3. Схема работы холодильной машины.
В этом случае рабочее тело расширяется вдоль кривой 1b 2, при этом выполняется положительная работа A 1 b 2 численно равная площади под кривой 1b 2. При сжатии рабочее тело возвращается в первоначальное состояние вдоль кривой 2a 1, при этом над ним совершается отрицательная работа A 2 a 1 численно равная площади под кривой 2a 1. Суммарная работа за цикл:
Это значит, что внешние силы совершают работу над рабочим телом. Такой круговой процесс называется обратным. В результате обратного цикла некоторое количество теплоты забирается у холодильника и передается нагревателю за счет работы внешних сил. Расширение рабочего тела происходит при более низкой температуре, чем сжатие. В результате некоторое количество теплоты забирается у холодного тела и передается горячему за счет работы внешних сил. Машина, которая работает по такому циклу, называется холодильной .
За счет работы внешних сил машина отдает больше тепла, чем получает:
![]() (3)
(3)
Работа такой машины характеризуется холодильным коэффициентом:
где Q 2 – теплота, отнятая от холодного тела, A – работа, выполненная над рабочим телом за цикл. Холодильный коэффициент больше единицы (тепловые насосы).
Теоретический анализ работы идеальной тепловой машины провел французский ученый Сади Карно в 1824 году. Он предложил круговой процесс (цикл) для работы идеальной тепловой машины, который складывается из двух изотерм и двух адиабат. Этот цикл называется циклом Карно . Цикл Карно сыграл важную роль в развитии теплотехники и термодинамики. Анализ этого цикла позволил улучшить работу тепловых машин, повысить их КПД .
Прямой цикл Карно складывается из четырех последовательных равновесных процессов рис.4.

Рис.4. Цикл Карно
1→2 - изотермическое расширение при температуре T 1 , 2→3 – адиабатное расширение, 3→4 – изотермическое сжатие при температуре T 2 , 4→1 – адиабатное сжатие. В машине, работающей по циклу Карно, отсутствуют потери энергии на теплопроводность, трение и т.д. Цикл Карно обратимый, потому что все процессы в нем квазистатические. С машиной связаны два тепловых резервуара. Один с температурой T 1 – нагреватель или теплоотдатчик, второй с более низкой температурой T 2 – холодильник или теплоприемник. Эти резервуары настолько велики, что отдача или прием теплоты практически не изменяют их температуры.
Определим работу, выполненную идеальным газом за один цикл Карно. При изотермическом процессе 1→2 T 1 = const, ΔU 12 = 0 и, согласно I началу термодинамики газу надо передать от нагревателя количество теплоты Q 1 , равное работе, которую газ выполняет при расширении:
 (5)
(5)
При адиабатном процессе 2→3, Q 23 = 0, температура газа понижается до T 2 , работа при расширении газа выполняется за счет уменьшения его внутренней энергии. Согласно I началу термодинамики:
![]()
Отсюда следует, что:
Изотермическое сжатие газа 3→4 выполняется за счет работы ты внешних сил. Чтобы температура газа осталась постоянной от него надо отнять количество теплоты Q 2 и передать ее холодильнику. Для изотермического процесса T 2 = const, ΔU 23 = 0 и, согласно I началу термодинамики.
Круговой процесс - процесс, при котором газ, пройдя через ряд состояний, возвращается в исходное.
Если круговой процесс на диаграмме P-V протекает по часовой стрелке, то часть тепловой энергии, полученной от нагревателя, превращается в работу. Так работает тепловая машина.
Если круговой процесс на диаграмме P-V протекает против часовой стрелки, то тепловая энергия передается от холодильника (тела с меньшей температурой) к нагревателю (телу с большей температурой) за счет работы внешней силы. Так работает холодильная машина.
Цикл Карно́ - идеальный термодинамический цикл . Тепловая машина Карно , работающая по этому циклу, обладает максимальным КПД из всех машин, у которых максимальная и минимальная температуры осуществляемого цикла совпадают соответственно с максимальной и минимальной температурами цикла Карно. Состоит из 2 адиабатических и 2 изотермических процессов .
Цикл Карно назван в честь французского военного инженера Сади Карно , который впервые его исследовал в 1824 году .
Одним из важных свойств цикла Карно является его обратимость: он может быть проведён как в прямом, так и в обратном направлении, при этом энтропияадиабатически изолированной (без теплообмена с окружающей средой) системы не меняется.
 | Цикл Карно состоит из четырёх стадий: 1. Изотермическое расширение (на рисунке - процесс A→Б). В начале процесса рабочее тело имеет температуру, то есть температуру нагревателя. Затем тело приводится в контакт с нагревателем, который изотермически (при постоянной температуре) передаёт ему количество теплоты . При этом объём рабочего тела увеличивается. 2. Адиабатическое (изоэнтропическое) расширение (на рисунке - процесс Б→В). Рабочее тело отсоединяется от нагревателя и продолжает расширяться без теплообмена с окружающей средой. При этом его температура уменьшается до температуры холодильника. 3. Изотермическое сжатие (на рисунке - процесс В→Г). Рабочее тело, имеющее к тому времени температуру, приводится в контакт с холодильником и начинает изотермически сжиматься, отдавая холодильнику количество теплоты . 4. Адиабатическое (изоэнтропическое) сжатие (на рисунке - процесс Г→А). Рабочее тело отсоединяется от холодильника и сжимается без теплообмена с окружающей средой. При этом его температура увеличивается до температуры нагревателя. |
Вычисление совершаемой веществом работы, за единичный цикл Карно при постоянных не одинаковых температурах Т1 и Т2 от нагревателя и холодильника, можно вычислить с помощью расчета:
А = Q1 - Q2 = (Т1-Т2/T1) *Q1 Данная работа количественно приравнивается к площади АВСD с ограничивающими отрезками в виде изотерм и адиабат которые и создают данный цикл.
Теорема Карно (с выводом).
Из всех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей T 1 и холодильников T 2 , наибольшим КПД обладают обратимые машины. При этом КПД обратимых машин, работающих при одинаковых температурах нагревателей и холодильников, равны друг другу и не зависят от природы рабочего тела, а определяются только температурами нагревателя и холодильника.
Для построения рабочего цикла использует обратимые процессы. Например, цикл Карно состоит из двух изотерм (1–2, 2-4) и двух адиабат (2-3, 4–1), в которых теплота и изменение внутренней энергии полностью превращаются в работу (рис. 19). 
Рис. 19. Цикл Карно
Общее изменение энтропии в цикле: ΔS=ΔS 12 +ΔS 23 +ΔS 34 +ΔS 41.
Так как мы рассматриваем только обратимые процессы, общее изменение энтропии ΔS=0.
Последовательные термодинамические процессы в цикле Карно:
Общее изменение энтропии в равновесном цикле: ΔS=(|Q 1 |/T 1)+0-(|Q 2 |/T 2)+0=0⇒T 2 /T 1 =|Q 2 |/|Q 1 |,
поэтому: η max =1-(T 2 /T 1) - максимальный КПД теплового двигателя.
Следствия:
1. КПД цикла Карно не зависит от рода рабочего тела.
2. КПД определяется только разницей температур нагревателя и холодильника.
3. КПД не может быть 100% даже у идеальной тепловой машины, так как при этом температура холодильника должна быть T 2 =0, что запрещено законами квантовой механики и третьим законом термодинамики.
4. Невозможно создать вечный двигатель второго рода, работающий в тепловом равновесии без перепада температур, т.е. при T 2 =T 1 , так как в этом случае η max =0.
II начало термодинамики.
Первое начало термодинамики, выражая закон сохранения и превращения энергии, не позволяет установить направление протекания термодинамических процессов. Кроме того, можно представить множество процессов, не противоречащих первому началу, в которых энергия сохраняется, а в природе они не осуществляются. Появление второго начала термодинамики связано с необходимостью дать ответ на вопрос, какие процессы в природе возможны, а какие нет. Второе начало термодинамики определяет направление протекания термодинамических процессов.
Используя понятие энтропии и неравенство Клаузиуса, второе начало термодинамики можно сформулировать как закон возрастания энтропии замкнутой системы при необратимых процессах: любой необратимый процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает.
Можно дать более краткую формулировку второго начала термодинамики: в процессах, происходящих в замкнутой системе, энтропия не убывает. Здесь существенно, что речь идет о замкнутых системах, так как в незамкнутых системах энтропия может вести себя любым образом (убывать, возрастать, оставаться постоянной). Кроме того, отметим еще раз, что энтропия остается постоянной в замкнутой системе только при обратимых процессах. При необратимых процессах в замкнутой системе энтропия всегда возрастает.
Формула Больцмана (2.134) позволяет объяснить постулируемое вторым началом термодинамики возрастание энтропии в замкнутой системе при необратимых процессах: возрастание энтропии означает переход системы из менее вероятных в более вероятные состояния. Таким образом, формула Больцмана позволяет дать статистическое толкование второго начала термодинамики. Оно, являясь статистическим законом, описывает закономерности хаотического движения большого числа частиц, составляющих замкнутую систему.
Укажем еще две формулировки второго начала термодинамики:
1) по Кельвину: невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу;
2) по Клаузиусу: невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому.
Можно довольно просто доказать эквивалентность формулировок Кельвина и Клаузиуса. Кроме того, показано, что если в замкнутой системе провести воображаемый процесс, противоречащий второму началу термодинамики в формулировке Клаузиуса, то он сопровождается уменьшением энтропии. Это же доказывает эквивалентность формулировки Клаузиуса (а следовательно, и Кельвина) и статистической формулировки, согласно которой энтропия замкнутой системы не может убывать.
В середине XIX в. возникла проблема так называемой тепловой смерти вселенной. Рассматривая Вселенную как замкнутую систему к применяя к ней второе начало термодинамики, Клаузиус свел его содержание к утверждению, что энтропия Вселенной должна достигнуть своего максимума. Это означает, что со временем все формы движения должны перейти в тепловую. Переход же теплоты от горячих тел к холодным приведет к тому, что температура всех тел во Вселенной сравняется, т. е. наступит полное тепловое равновесие и все процессы во Вселенной прекратятся – наступит тепловая смерть Вселенной. Ошибочность вывода о тепловой смерти заключается в том, что бессмысленно применять второе начало термодинамики к незамкнутым системам, например к такой безграничной в бесконечно развивающейся системе, как Вселенная.
Энтропия по Клаузиусу.
К макроскопическим параметрам термодинамической системы относятся давление, объём и температура. Однако существует ещё одна важная физическая величина, которую используют для описания состояний и процессов в термодинамических системах. Её называют энтропией.
Впервые это понятие ввёл в 1865 г. немецкий физик Рудольф Клаузиус. Энтропией он назвал функцию состояния термодинамической системы, определяющую меру необратимого рассеивания энергии.
Что же такое энтропия? Прежде чем ответить на этот вопрос, познакомимся с понятием «приведенной теплоты». Любой термодинамический процесс, проходящий в системе, состоит из какого-то количества переходов системы из одного состояния в другое. Приведенной теплотой называют отношение количества теплоты в изотермическом процессе к температуре, при которой происходит передача этой теплоты.
Q" = Q/T .
Для любого незамкнутого термодинамического процесса существует такая функция системы, изменение которой при переходе из одного состояния в другое равно сумме приведенных теплот. Этой функции Клаузиус дал название «энтропия » и обозначил её буквой S , а отношение общего количества теплоты ∆Q к величине абсолютной температурыТ назвал изменением энтропии .
Обратим внимание на то, что формула Клаузиуса определяет не само значение энтропии, а только её изменение.
Что же представляет собой «необратимое рассевание энергии» в термодинамике?
Одна из формулировок второго закона термодинамики выглядит следующим образом: "Невозможен процесс, единственным результатом которого является превращение в работу всего количества теплоты, полученного системой ". То есть часть теплоты превращается в работу, а какая-то её часть рассеивается. Этот процесс необратим. В дальнейшем рассеиваемая энергия уже не может совершать работу. Например, в реальном тепловом двигателе рабочему телу передаётся не вся теплота. Часть её рассеивается во внешнюю среду, нагревая её.
В идеальной тепловой машине, работающей по циклу Карно, сумма всех приведенных теплот равна нулю. Это утверждение справедливо и для любого квазистатического (обратимого) цикла. И неважно, из какого количества переходов из одного состояния в другое состоит такой процесс.
Если разбить произвольный термодинамический процесс на участки бесконечно малой величины, то приведенная теплота на каждом таком участке будет равна δQ/T . Полный дифференциал энтропии dS = δQ/T .
Энтропию называют мерой способности теплоты необратимо рассеиваться. Её изменение показывает, какое количество энергии беспорядочно рассеивается в окружающую среду в виде теплоты.
В замкнутой изолированной системе, не обменивающейся теплом с окружающей средой, при обратимых процессах энтропия не изменяется. Это означает, что дифференциал dS = 0 . В реальных и необратимых процессах передача тепла происходит от тёплого тела к холодному. В таких процессах энтропия всегда увеличивается (dS ˃ 0 ). Следовательно, она указывает направление протекания термодинамического процесса.
Формула Клаузиуса, записанная в виде dS = δQ/T , справедлива лишь для квазистатических процессов. Это идеализированные процессы, являющиеся чередой состояний равновесия, следующих непрерывно друг за другом. Их ввели в термодинамику для того, чтобы упростить исследования реальных термодинамических процессов. Считается, что в любой момент времени квазистатическая система находится в состоянии термодинамического равновесия. Такой процесс называют также квазиравновесным.
Конечно, в природе таких процессов не существует. Ведь любое изменение в системе нарушает её равновесное состояние. В ней начинают происходить различные переходные процессы и процессы релаксации, стремящиеся вернуть систему в состояние равновесия. Но термодинамические процессы, протекающие достаточно медленно, вполне могут рассматриваться как квазистатические.
На практике существует множество термодинамических задач, для решения которых требуется создание сложной аппаратуры, создание давления в несколько сот тысяч атмосфер, поддержание очень высокой температуры в течение длительного времени. А квазистатические процессы позволяют рассчитать энтропию для таких реальных процессов, предсказать, как может проходить тот или иной процесс, реализовать который на практике очень сложно.
Второе начало термодинамики: Невозможно построить периодически действующую тепловую машину, которая бы всю подводимую к ней теплоту превращала в работу, т.е. всегда .
Французский инженер Сади Карно предложил идеальный цикл, который даёт максимальное значение КПД. Этот цикл состоит из двух изотерм и двух адиабат и носит название цикла Карно .
| - изотермическое расширение при , - адиабатическое расширение , - изотермическое сжатие при , - адиабатическое сжатие . |
 Рис. 2.2 Цикл Карно в координатах (P, V).
Рис. 2.2 Цикл Карно в координатах (P, V).
Вычислим КПД цикла Карно для идеального газа. При изотермическом процессе внутренняя энергия идеального газа остаётся постоянной. Поэтому количество полученной газом теплоты равно работе , совершаемой газом при переходе из состояния 1 в состояние 2 (рис. 2.2). Эта работа равна ![]() где – масса идеального газа в тепловой машине.
где – масса идеального газа в тепловой машине.
Количество отдаваемой холодильнику теплоты равно работе , затраченной на сжатие газа при переходе его из состояния 3 в состояние 4. Эта работа равна![]() .
.
Для того, чтобы цикл был замкнутым, состояние 1 и 4 должны лежать на одной и той же адиабате. Отсюда вытекает условие:
![]() .
.
Аналогично для состояний 2 и 3 справедливо условие:
![]() .
.
Разделив одно соотношение на другое, приходим к условию замкнутости цикла :
Подставляя и в выражение для КПД, получим:
![]() . (2.2)
. (2.2)
В результате получим формулу для КПД цикла Карно:
где - температура нагревателя, - температура холодильника. КПД цикла Карно является максимальным КПД из всех возможных циклов, осуществляемых в данных температурных интервалах и .
Соотношение (2.2) составляет содержание теоремы Карно для обратимого цикла :
![]() .
.
Для необратимого цикла теорема Карно принимает вид:
![]() .
.
В общем случае можно объединить эти две записи теоремы Карно :
![]() . (2.3)
. (2.3)
Преобразуем (2.3) следующим образом:
В результате получим
Для обратимого цикла Карно: ,
для необратимого цикла Карно: .
Тогда в случае произвольного обратимого цикла можно получить:
а в случае произвольного необратимого цикла:
Соотношение (2.4) показывает, что величина, стоящая под знаком интеграла, является функцией состояния. Эта функция состояния обозначается буквой S и называется энтропией . Наряду с внутренней энергией U энтропия S играет важную роль в термодинамике.
Конец работы -
Эта тема принадлежит разделу:
Основные положения молекулярно-кинетической теории. Масса и размер молекул
М к т изучает свойства вещества давление температуру и так далее как суммарный результат действий молекул при этом пользуется статическим..
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ:
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Все темы данного раздела:
Основные положения молекулярно-кинетической теории
1. Все вещества состоят из мельчайших частиц - атомов и молекул.
2. Молекулы и атомы любого вещества находятся в непрерывном хаотическом движении, которое называется тепловым движением
Масса и размеры молекул
Для характеристики масс атомов и молекул применяются следующие величины:
Атомная масса – масса атома вещества, выраженная в а.е.м.
Молекулярная масса – масса
Термодинамические параметры и процессы. Урав-е сост-я идеального газа
Для описания состояния термодинамической системы вводятся физические величины, которые называются термодинамическими параметрами или параметрами состояния системы. Обычно в качестве термодин
Основное ур-е молекулярно-кинетической теории гага
1) Молекулы газа движутся только вдоль трех взаимно перпендикулярных направлений. Если в сосуде содержится N молекул, то в любой момент времени вдоль каждой из осей координат будет двигаться
Закон равномерного распределения энергии по степеням свободы. Внутренняя энергия ИГ
Числом степеней свободы i системы называется количество независимых величин, с помощью которых может быть задано положение системы. Так, положение в пространстве материальной точки полностью
Максвелловское распределение энергии по степеням свободы молекул газа. Внутренняя энергия идеального газа
В случае идеального газа число молекул в единице объема, имеющих значение компоненты скорости в интервале от vx до vx + dvx может быть представ
Характерные скорости молекул газа. Опыт Штерна
1.-наиболее вероятная скорость молекул
Больцмановское распределение частиц газа по потенциальной энергии. Распределение Максвелла-Больцмана
Если газ находится во внешнем силовом поле, то частицы газа обладают потенциальной энергией eп. Распределение молекул идеального газа по высоте в однородном гравитационном поле.
Средняя длина свободного пробега молекул газа. Понятие о вакууме
Под средней длиной свободного пробега понимают среднее расстояние, которое проходит молекула между двумя последовательными соударениями.
За секунду молекула в среднем проходит расстояние,
Явление переноса: теплопроводность ИГ
Явления переноса в газах. Общие закономерности.
Беспорядочность теплового движения молекул газа, непрерывные соударения между ними приводят к постоянному перемешиванию частиц и изменению и
Диффузия и внутреннее трение в идеальном газе
Явление переноса - диффузия - заключается в самопроизвольном взаимном проникновении и перемешивании частиц двух соприкасающихся газов, жидкостей и даже твердых тел. При этом различают самодиффузию
Первое начало термодинамики. Теплоемкость ИГ. Работа газа при изменении его объема
Первое начало термодинамики:
Количество теплоты, сообщённое газу, идёт на приращение внутренней энергии газа и на совершенигазом работы над внешними телами.
Термодинамика изохорического процесса: V=const
Рассмотрим закон, описывающий этот процесс, и его график в координатах (P,V). Этот закон является частным случаем уравнения Менделеева-Клапейрона (уравнения состояния идеального газа)
Термодинамика изотермического процесса: T=const
Приведем закон, описывающий этот процесс, и его график в координатах (P,V). Рассмотрев два состояния идеального газа 1 и 2, получим
Термодинамика адиабатического процесса: dQ=0
Адиабатический процесс - это процесс, протекающий без теплообмена с окружающей средой.
Поскольку dQ = 0, то первое начало термодинамики принимает вид:
Политропические процессы
Политропическими процессами называются процессы, при которых теплоемкость газа остается постоянной.
Найдем уравнение состояния идеального газа при политропическом процессе, т.е. уравнение
Энтропия и 2-е начало трмодинамики
Энтропия – это такая функция состояния, дифференциал которой определяется отношением:
Реальный газ. Уравнение Ван-дер-Ваальса и его анализ. Критическое состояние и его параметры
Реальный газ - газ, который не описывается уравнением состояния идеального газа Клапейрона - Менделеева.
Зависимости между его параметрами показывают, что молекулы в реальном газе взаимоде














